Регулация на генната експерсия – Тематични направления
Молекулярни и клетъчно-биологични механизми, свързани с постембрионалното развитие на растенията
Постембрионално развитие на кореновата система
Изследване на вътреклетъчния мембранен трафик в растителните клетки чрез нови химични модулатори
Клетъчна, тъканна и органна специфичност на хормоналните сигнали и взаимодействия
Епигенетична регулация на генната експресия
Влияние на епигенетичните модификации на ДНК върху развитието и отговора на растенията към абиотичен стрес
Проучване на генните функции в хетероложни системи
Структурна организация на растителния геном в условия на абиотичен стрес
Генотоксична оценка на растителния геном в условия на абиотичен стрес
Молекулна и фенотипна характеристика на растенията в условия на абиотичен стрес
Молекулни и фенотипни маркери за изследване на генетичните основи на толерантността на растенията към абиотичен стрес
Изменения в количеството и активността на ключови белтъци при стресови въздействия. Протеомен анализ
Молекулярни и клетъчно-биологични механизми, свързани с постембрионалното развитие на растенията
Постембрионално развитие на кореновата система
Проучват се гени и сигнални пътища, включени във формирането на кореновата система при моделното растение Arabidopsis thaliana и културни растения като пшеница, камелина и др. Особено внимание се отделя на идентифицирането на ранни регулатори, контролиращи спецификацията на иницииращите клетки и последващите структурирани асиметрични и симетрични клетъчни деления, водещи до образуване на латерални коренови зачатъци и разклоняване на кореновата система. Изследва се ауксин-зависимата миграция на клетъчното ядро в иницииращите клетки, която е важна предпоставка за асиметричните клетъчни деления. Всички етапи на коренообразуването се контролират от фитохормона ауксин и проучването на ключови компоненти от ауксиновата сигнализация e важен елемент от разбирането на адаптационните промени в хода на развитието на растенията и при неблагоприятни фактори на средата.
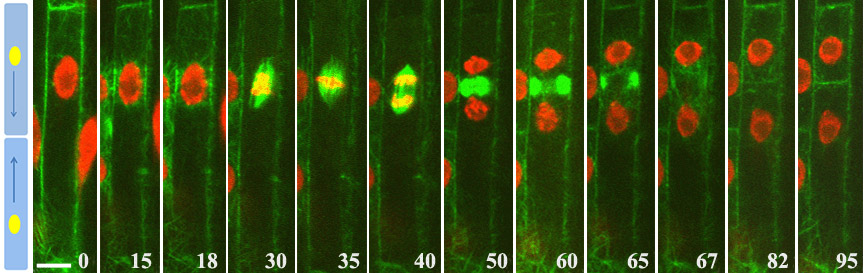
Поляризиране и асиметрични клетъчни деления на иницииращи клетки от кореновия перицикъл на Arabidopsis thaliana
Прочетете повече
- Velinov V, Zehirov G, Georgieva M, Vassileva V. 2021. NUDC-like genes contribute to root growth and branching in Arabidopsis thaliana. R. Acad. Bulg. Sci. 74, 12, 1767-1773.
- Velinov V, Georgieva M, Vangheluwe N, Beeckman T, Vassileva V. 2020. Overexpression of the NMig1 gene encoding a NudC domain protein enhances root growth and abiotic stress tolerance in Arabidopsis thaliana. Frontiers in Plant Science 11, 815.
- Fernandez A, Drozdzecki A, Hoogewijs K, Vassileva V, Madder A, Beeckman T, Hilson P. 2015. The GLV6/RGF8/CLEL2 peptide regulates early pericycle divisions during lateral root initiation. Journal of Experimental Botany 17, 5245-5256.
- Chen Q, Liu Y, Maere S, Lee E, Van Isterdael G, Xie Z, Xuan W, Lucas J, Vassileva V, Kitakura S, Marhavý P. 2015. A coherent transcriptional feed-forward motif model for mediating auxin-sensitive PIN3 expression during lateral root development. Nature Communications 6, 8821.
- Boycheva I, Vassileva V, Revalska M, Zehirov G, Iantcheva A. 2015. Cyclin-like F-box protein plays a role in growth and development of the three model species Medicago truncatula, Lotus japonicus and Arabidopsis thaliana. Research and Reports in Biology 6, 117-130.
- Revalska M, Vassileva V, Zehirov G, Iantcheva I. 2015. Is the auxin influx carrier LAX3 essential for plant growth and development in the model plants Medicago truncatula, Lotus japonicus and Arabidopsis thaliana? Biotechnology & Biotechnological Equipment 29, 4, 786-797.
- Berckmans B, Vassileva V, Schmid S, Maes S, Parizot B, Naramoto S, Magyar Z, Kamei CLA, Koncz C, Persiau G, De Jaeger G, Bogre L, Friml J, Simon R, Beeckman T, De Veylder L. 2011. Auxin-dependent cell cycle reactivation through transcriptional control of E2Fa by LATERAL ORGAN BOUNDARY proteins. Plant Cell 23, 10, 3671-3683.
- De Rybel B, Vassileva V, Parizot B, Demeulenaere M, Grunewald W, Audenaert D, Van Campenhout J, Overvoorde P, Jansen L, Vanneste S, Möller B, Holman T, Van Isterdaele G, Brunoud G, Vuylsteke M, Vernoux T, De Veylder L, Inzé D, Weijers D, Bennett M, Beeckman T. 2010. A novel Aux/IAA28 signalling cascade activates GATA23-dependent specification of lateral root founder cell identity. Current Biology 20, 19, 1697-1706.
- De Smet I, Vassileva V, De Rybel B, Levesque MP, Grunewald W, Van Damme D, Van Noorden G, Naudts M, Van Isterdael G, De Clercq R, Wang JY, Meuli N, Vanneste S, Friml J, Hilson P, Jürgens G, Ingram GC, Inzé D, Benfey PN, Beeckman T. 2008. Receptor-like kinase ACR4 restricts stem cell divisions in the Arabidopsis Science 322, 5901, 594-597.
[ Top ]
Изследване на вътреклетъчния мембранен трафик в растителните клетки чрез нови химични модулатори
За изучаване на функционалната взаимовръзка между ендомембранния трафик и фитохормоналните вериги за сигнална трансдукция могат успешно да бъдат използвани нискомолекулни химични съединения, идентифицирани чрез широкомащабен скрининг на синтетични химични библиотеки. С помощта на химичната генетика могат да бъдат преодолени съществени недостатъци на класическия генетичен подход, каквито са леталният характер на много от мутациите и липсата на специфичен фенотип в резултат на припокриване на генетични функции. Ключово предимство на този подход при анализирането на комплексни и силно динамични биологични процеси, какъвто е вътреклетъчният мембранен трафик, е огромното разнообразие от химични структури, които могат да бъдат използвани за изучаване на функциите на растителните белтъци, към които съединенията обратимо се свързват. Основно предизвикателство пред растителната химична генетика е идентифицирането на белтъчните мишени на биоактивните съединения, което е от съществено значение за изясняване на механизмите на действие на малките молекули и тяхната специфичност.
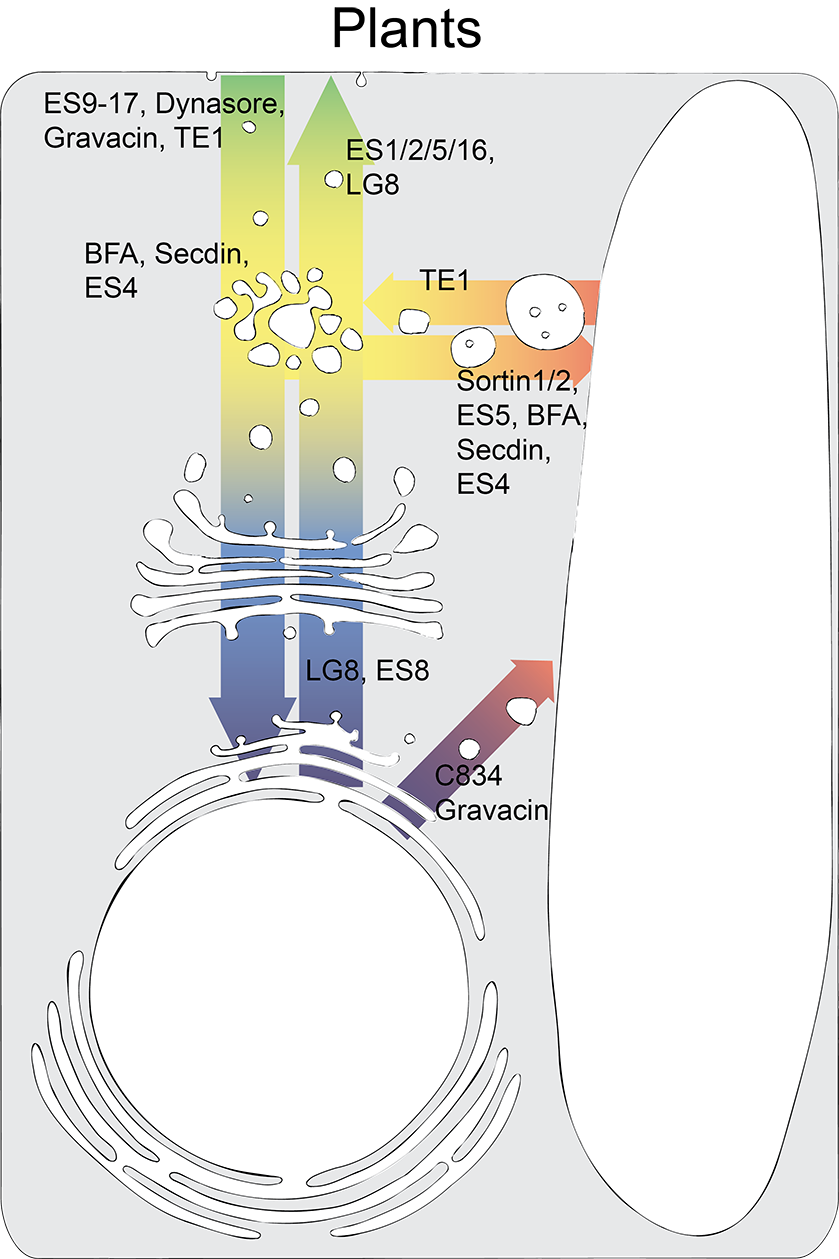
Схематично представяне на главните пътища на вътреклетъчен мембранен трафик и известните до момента нискомолекулни инхибитори на трафика в растителните клетки (Chem Biol 20, 2013, 475-486, с допълнения).
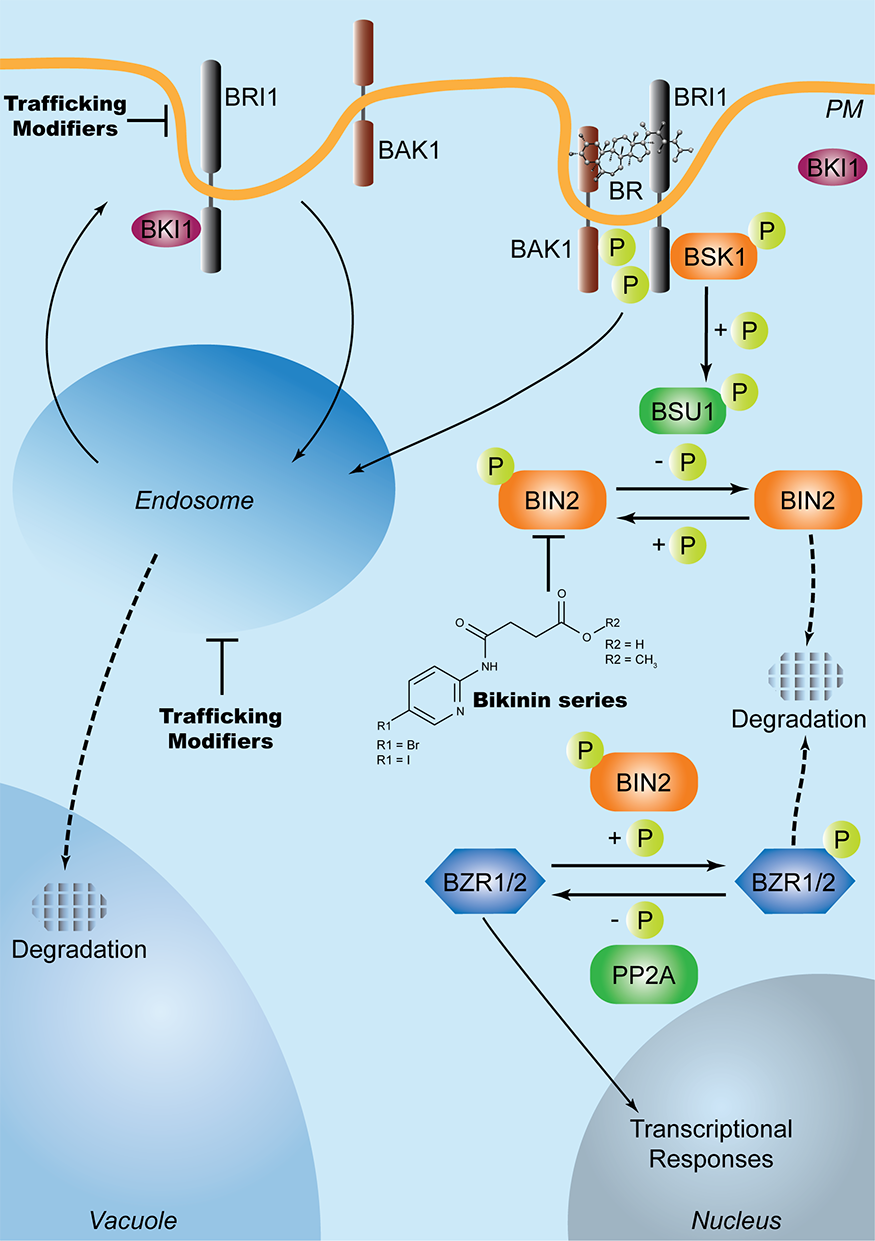
Взаимовръзка между вътреклетъчния мембранен трафик и фитохормоналните сигнални пътища. Пример, илюстриращ директния ефект на ендоцитозата върху сигналните пътища на ендогенни растежни регулатори, е трафикът на брасиностероидния рецептор BRASSINOSTEROID INSENSITIVE1 (BRI1), който непрекъснато се придвижва от плазмената мембрана към ендозомите и обратно (Curr Opin Plant Biol 22, 48-55).
Прочетете повече
- Dejonghe W, Sharma I, Denoo B, De Munck S, Lu Q, Mishev K, Bulut H, Mylle E, De Rycke R, Vasileva M, Savatin DV, Nerinckx W, Staes A, Drozdzecki A, Audenaert D, Yperman K, Madder A, Friml J, Van Damme D, Gevaert K, Haucke V, Savvides SN, Winne J, Russinova E. 2019. Disruption of endocytosis through chemical inhibition of clathrin heavy chain function. Nature Chemical Biology, 15(6): 641-649.
- Mishev K, Lu Q, Denoo B, Peurois F, Dejonghe W, Hullaert J, De Rycke RM, Boeren S, Bretou M, De Munck S, Sharma IS, Goodman K, Kalinowska K, Storme V, Nguyen L, Drozdzecki A, Martins S, Nerinckx W, Audenaert D, Vert G, Madder A, Otegui MS, Isono E, Savvides S, Annaert W, de Vries SC, Cherfils J, Winne J, Russinova E. Nonselective chemical inhibition of Sec7 domain-containing ARF GTPase exchange factors. The Plant Cell, 30(10): 2573-2593.
- Kania U, Nodzynski T, Lu Q, Hicks GR, Nerinckx W, Mishev K, Peurois F, Cherfils J, De Rycke RM, Grones P, Robert S, Russinova E, Friml J. 2018. The inhibitor Endosidin 4 targets SEC7 domain-type ARF GTPase exchange factors and interferes with subcellular trafficking in eukaryotes. The Plant Cell, 30(10): 2553-2572.
- Dejonghe W, Kuenen S, Mylle E, Vasileva M, Keech O, Viotti C, Swerts J, Fendrych M, Ortiz-Morea FA, Mishev K, Delang S, Scholl S, Zarza X, Heilmann M, Kourelis J, Kasprowicz J, Nguyen le SL, Drozdzecki A, Van Houtte I, Szatmári AM, Majda M, Baisa G, Bednarek SY, Robert S, Audenaert D, Testerink C, Munnik T, Van Damme D, Heilmann I, Schumacher K, Winne J, Friml J, Verstreken P, Russinova E. 2016. Mitochondrial uncouplers inhibit clathrin-mediated endocytosis largely through cytoplasmic acidification. Nature Communications 7, 11710.
- Dejonghe W, Mishev K, Russinova E. The brassinosteroid chemical toolbox. Current Opinion in Plant Biology 22, 48-55.
- Mishev K, Dejonghe W, Russinova E. Small molecules for dissecting endomembrane trafficking: a cross-systems view. Chemistry & Biology 20, 2013, 475-486.
- Irani N, Di Rubbo S, Mylle E, Van den Begin J, Schneider-Pizoń J, Hniliková J, Šíša M, Buyst D, Buyst D, Vilarrasa-Blasi J, Szatmári AM, Van Damme D, Mishev K, Codreanu MC, Kohout L, Strnad M, Caño-Delgado AI, Friml J, Madder A, Russinova E. Fluorescent castasterone reveals BRI1 signaling from the plasma membrane. Nature Chemical Biology 8, 6, 583-589.
[ Top ]
Клетъчна, тъканна и органна специфичност на хормоналните сигнали и взаимодействия
Клетъчното делене и нарастване, стоящи в основата на увеличаването на размера на растителните органи, се контролират от специфични хормони. Различните сигнални пътища сформират от своя страна сложно устроена регулаторна система, която контролира множество физиологични и биохимични процеси в отговор на различни екзогенни и ендогенни стимули. Установено е, че отделни видове клетки имат водеща роля при приемането и преноса на конкретни хормонални сигнали, регулиращи физиологичните и биохимични процеси в растителния организъм. По-доброто разбиране на механизмите, чрез които различните хормони координират действието си в отделните растителни тъкани и органи, за да ограничат или стимулират растежа при нормални или неблагоприятни условия на околната среда, подпомага разработването на молекулни стратегии за създаване на устойчиви към стрес растения. При тези изследвания широко приложение намират различни мутантни и репортерни линии, както и трансгенни растения с насочена експресия, съдържащи клетъчно-специфични генни промотори.
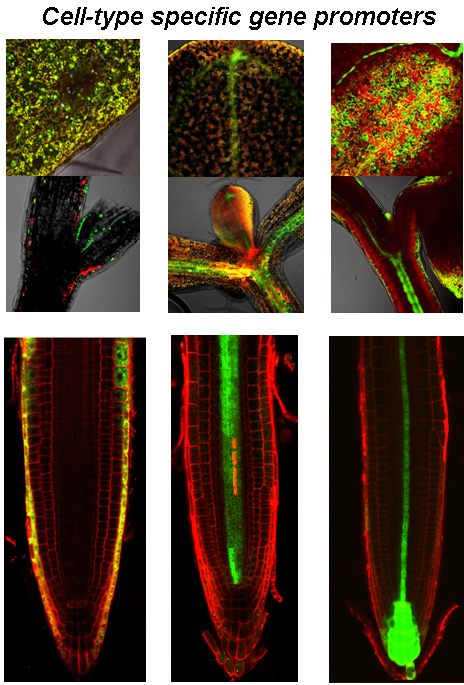
Натрупаните знания в хода на експерименталната работа биха били полезни за разработването на нови биотехнологични инструменти и стратегии за прецизирана манипулация на регулаторните механизми на растежа, което може да увеличи устойчивостта към стрес и да подобри желани характеристики в икономически важни култури.
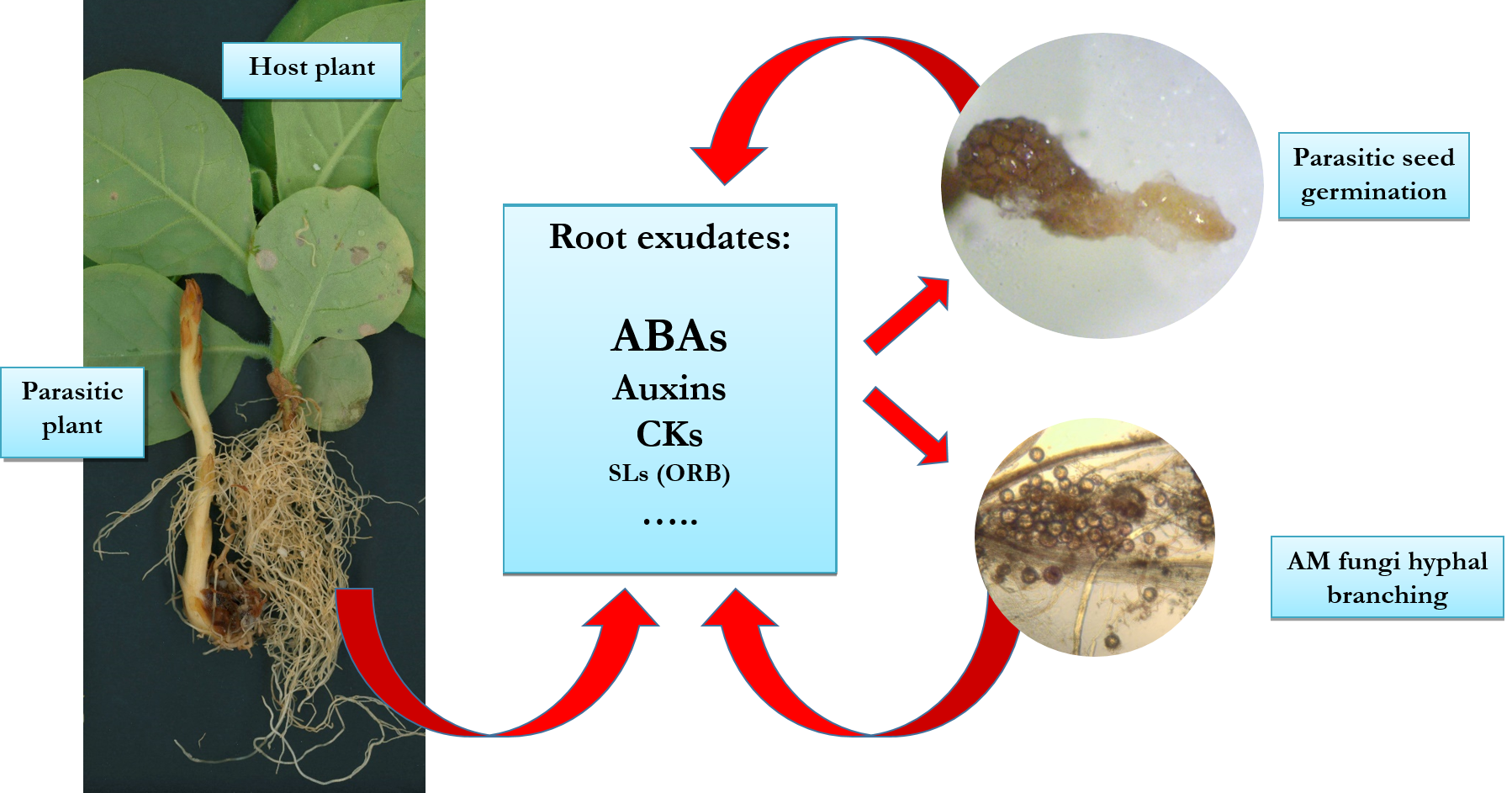
Подземни взаимодействия между растение-гостоприемник, паразитно растение и арбускуларно-микоризни гъби (АМГ), свързани с промени в хормоналната регулация. Съвместното отглеждане на тютюневи растения със синя китка от род Phelipanche самостоятелно или в комбинация с АМГ от вида Rhizophagus irregularis води до характерни изменения в нивата на редица фитохормони в корените на гостоприемника и в кореновите отделяния, които от своя страна повлияват растежа на гостоприемника и устойчивостта му към стресови въздействия от средата.
Прочетете повече
- Mishev K, Dobrev PI, Lacek J, Filepova R, Yuperlieva-Mateeva B, Kostadinova A, Hristeva T, 2021. Hormonomic changes driving the negative impact of broomrape on plant host interactions with arbuscular mycorrhizal fungi. International Journal of Molecular Sciences, 22(24): 13677.
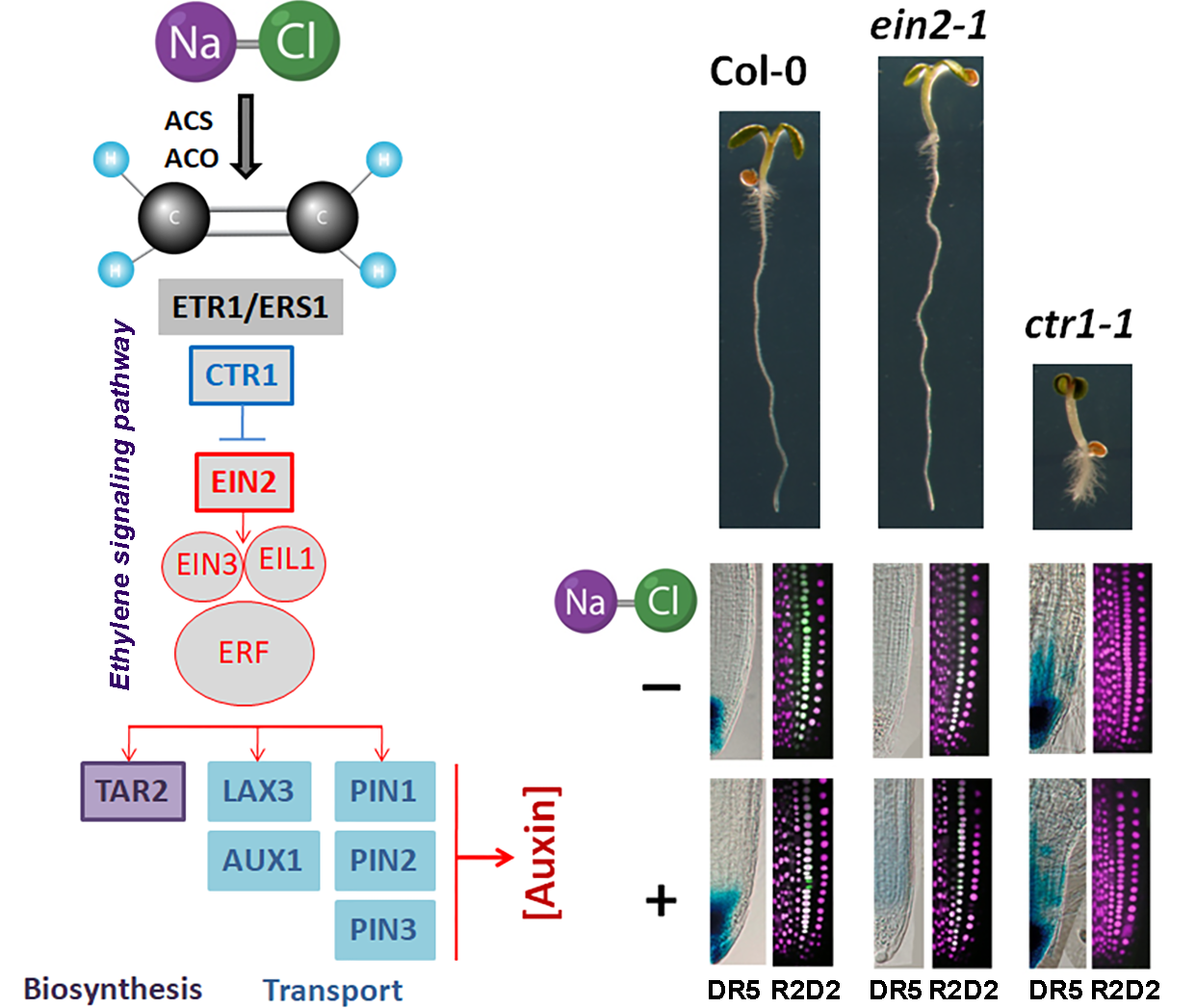
- Vaseva II., Simova-Stoilova L, Kirova E, Mishev K, Depaepe T, Van Der Straeten D, Vassileva V, 2021. Ethylene signaling in salt-stressed Arabidopsis thaliana ein2-1 and ctr1-1 mutants – A dissection of molecular mechanisms involved in acclimation. Plant Physiology and Biochemistry, 167: 999-1010.
- Vaseva II, Mishev K, Depaepe T, Vassileva V, Van Der Straeten D, 2021. The diverse salt-stress response of Arabidopsis ctr1-1 and ein2-1 ethylene signaling mutants is linked to altered root auxin homeostasis. Plants, 10(3): 452.
- Vaseva II, Qudeimat E, Potuschak T, Du Y, Genschik P, Vandenbussche F, Van Der Straeten D. 2018. The plant hormone ethylene restricts Arabidopsis growth via the epidermis. Proceedings of the National Academy of Sciences of the United States of America, 115 (17): E4130-E4139.
- Zhou J, Liu D, Wang P, Ma X, Lin W, Chen S, Mishev K, Lu D, Kumar R, Vanhoutte I, Meng X, He P, Russinova E, Shan L. 2018. Regulation of Arabidopsis brassinosteroid receptor BRI1 endocytosis and degradation by plant U-box PUB12/PUB13-mediated ubiquitination. Proceedings of the National Academy of Sciences of the United States of America, 115(8): E1906-1915.
- Vaseva II, Vandenbussche F, Simon D, Vissenberg K, Van Der Straeten D. 2016. Cell type specificity of plant hormonal signals: Case studies and reflections on ethylene. Russian Journal of Plant Physiology, 63, 5, DOI:10.1134/S1021443716050149, 577-586.
- Vandenbussche F, Vaseva I, Vissenberg K, Van Der Straeten D. Ethylene in vegetative development: a tale with a riddle. New Phytologist 194, 4, 895-909.
- Vaseva I, Todorova D, Malbeck J, Trávníčková A, Macháčková I. Response of cytokinin pool and cytokinin oxidase/dehydrogenase activity to abscisic acid exhibits organ specificity in peas. Acta Physiologiae Plantarum 30 (2): 151-155
- Todorova D, Vaseva I, Malbeck J, Trávníčková A, Macháčková I, Karanov E. 2007. Cytokinin oxidase/dehydrogenase activity as a tool in gibberellic acid/cytokinin cross talk. Biol. Plantarum51 (3): 579-583.
- Vaseva-Gemisheva I, Todorova D, Malbeck J, Travnickova A, Machackova I, Karanov E. 2006. Cytokinin pool dynamic changes and distribution of cytokinin oxidase/dehydrogenase activity in peas in relation to developmental senescence. Comp. Rend. Bulg. Acad. Sci. 59 (1): 65-70.
[ Top ]
Епигенетична регулация на генната експресия
Влияние на епигенетичните модификации на ДНК върху развитието и отговора на растенията към абиотичен стрес
Епигенетичните модификации активират или деактивират определени гени или участъци от молекулата на ДНК без промяна в нуклеотидната последователност, което осигурява гъвкава и обратима регулация на генната експресия. Тази регулация се осъществява чрез метилиране на ДНК, хистонови модификации и некодиращи РНКи (ncRNA), които определят компактизацията на хроматина. Анализират се епигенетично променени участъци от генома, стабилността на промените и тяхното унаследяване, както и активността на индивидуални гени. Проучват се ефектите на редуцираното/липсващо метилиране и комплементационното му възстановяване чрез директен трансфер на ДНК или генетични кръстоски, като се търси взаимовръзка между фенотипните промени в растенията и промените в генната експресия, индуцирани от епигенетични модификации в растителния геном. Проучва се взаимовръзката между промените в метилирането на ДНК и адаптацията на растенията към абиотичен стрес. Унаследяемите промени в метилирането са важна предпоставка за трайни адаптационни изменения за оцеляване на растенията в екстремни условия. Степента на метилиране на стрес-индуцируеми гени при моделни растения, както и при толерантни и чувствителни към засушаване сортове и линии пшеница, се изследва чрез метода на бисулфитната модификация на ДНК и метилационно-чувствителни рестрикционни анализи.
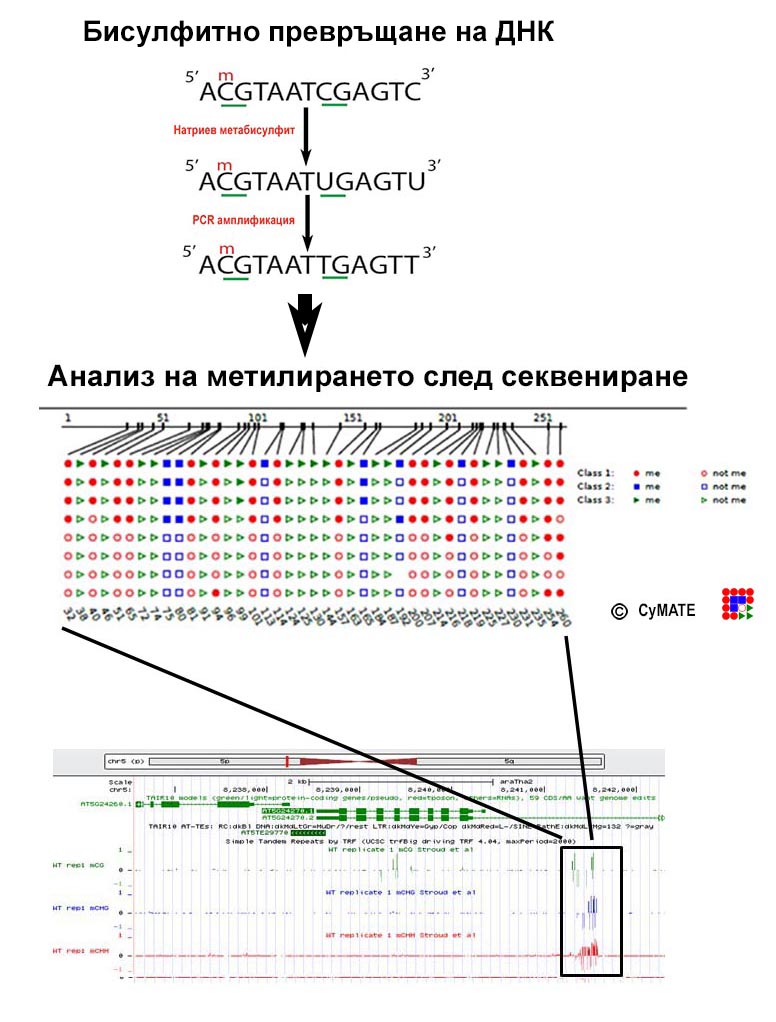
Анализ на метилирането на промотора на метилиран ген чрез бисулфитно превръщане и последващо секвениране.
Прочетете повече
- Boycheva I, Bonchev G, Manova V, Stoilov L, Vassileva V. How histone acetyltransferases shape plant photomorphogenesis and UV response. International Journal of Molecular Sciences, 25, 14, 7851.
- Agius DR, Kapazoglou A, Avramidou E, Baranek M, Carneros E, Caro E, Castiglione S, Cicatelli A, Radanovic A, Ebejer J-P, Gackowski D, Guarino F, Gulyas A, Hidvegi N, Hoenicka H, Inacio V, Johannes F, Karalija E, Lieberman-Lazarovich M, Martinelli F, Maury S, Mladenov V, Morais-Cecılio L, Pecinka A, Tani E, Testillano PS, Todorov D, Valledor L, Vassileva V. 2023. Exploring the crop epigenome: a comparison of DNA methylation profiling techniques. Front. Plant Sci., 14, 1-25.
- Kakoulidou I, Avramidou EV, Baránek M, Brunel-Muguet S, Farrona S, Johannes F, Kaiserli E, Lieberman-Lazarovich M, Martinelli F, Mladenov V, Testillano PS, Vassileva V, Maury S. 2021. Epigenetics for crop improvement in times of global change. Biology, 10, 8, 766
- Mladenov V, Fotopoulos V, Kaiserli E, Karalija E, Maury S, Baranek M, Segal N, Testillano PS, Vassileva V, Pinto G, Nagel M, Hoenicka H, Miladinović D, Gallusci P, Vergata C, Kapazoglou A, Abraham E, Tani E, Gerakari M, Sarri E, Avramidou Е, Gašparović M, Martinelli F. 2021. Deciphering the epigenetic alphabet involved in transgenerational stress memory in crops. International Journal of Molecular Sciences, 22, 13, 7118
- Boycheva I, Vassileva V, Revalska M, Zehirov G, Iantcheva A. 2017. Role of the histone acetyltransferase HAC1 gene in development of the model species Medicago truncatula, Lotus japonicus and Arabidopsis thaliana. Protoplasma 254, 2, 697-711
- Vassileva V, Hollwey E, Todorov D, Meyer P. 2016. Leaf epidermal profiling as a phenotyping tool for DNA methylation mutants. Genetics and Plant Physiology 6, 1-2, 3-13
- Boycheva I, Vassileva V, Iantcheva A. 2014. Histone acetyltransferases in plant development and plasticity. Current Genomics 15, 1, 28-3
[ Top ]
Проучване на генните функции в хетероложни системи
Използват се моделни растения като алтернативни експериментални системи за проучване на функциите на гени с висока степен на еволюционна консервативност. Редица заболявания при човека са свързани с генни мутации, чийто летален ефект затруднява тяхното изследване. Растенията предлагат добра алтернатива, тъй като в много случаи са по-толерантни към мутации, в сравнение с животинските организми. За разлика от бозайниците, моделното растение A. thaliana толерира мутации в епигенетичните системи и може да преживява и дава поколение при загуба/редукция на метилирането. По тази причина, използваме това растение като експериментален модел за проучване на степента на консервативност и дивергентност в системите за специфично CG метилиране. Изследва се възможността за функционална взаимозаменяемост на DNMT1 и MET1, които изпълняват ключова роля в поддържащото метилиране, съответно в бозайници и растения.
Проучваме, също така, еволюционно консервативни гени, кодиращи нискомолекулни протеини с NudC домен, които функционират не само като молекулни шаперони, но имат важна роля в развитието на организмите. Семейството на NudC протеините присъства във всички еукариоти, включително и в човек, което предполага важни фукции, запазени в хода на еволюцията. Обект на нашето изследване са NudC гените от A. thaliana, като се търси и функционална хомология между растителните NudC и гени от дрожди (Saccharomyces cerevisiae).

Хипотетичен модел, илюстриращ известните и предполагаемите функции на NudC гените в различни еукариоти (Plants 2024, 13, 119)
Прочетете повече
- Vassileva V, Georgieva M, Todorov D, Mishev K. 2024. Small sized yet powerful: Nuclear Distribution C proteins in plants. Plants, 13, 1, 119.
- Velinov V, Georgieva M, Zehirov G, Vassileva V. NudC-like genes contribute to root growth and branching in Arabidopsis thaliana. Comptes Rendus de L’Academie Bulgare Des Sciences, 74, 12, 1767-1773.
- Velinov V, Vaseva I, Zehirov G, Zhiponova M, Georgieva M, Vangheluwe N, Beeckman T, Vassileva V. 2020. Overexpression of the NMig1 gene encoding a NudC domain protein enhances root growth and abiotic stress tolerance in Arabidopsis thaliana. Frontiers in Plant Science, 11, 815
[ Top ]
Структурна организация на растителния геном в условия на абиотичен стрес
Генотоксична оценка на растителния геном в условия на абиотичен стрес
Извършва се оценка на генотоксичните ефекти на различни абиотични стресови фактори от околната среда като йонизираща радиация, UV радиация, химикали, пестициди, фитокомпоненти, тежки метали, наночастици и др. Възникналите повреди в ДНК на растенията служат като неспецифичен биомаркер за състоянието на средата и за предсказване на последиците от различни замърсявания. Анализът на възникналите първични повреди в ДНК (едно- и двойно-верижни скъсвания) и тяхното възстановяване се извършва с помощта на кометен анализ.
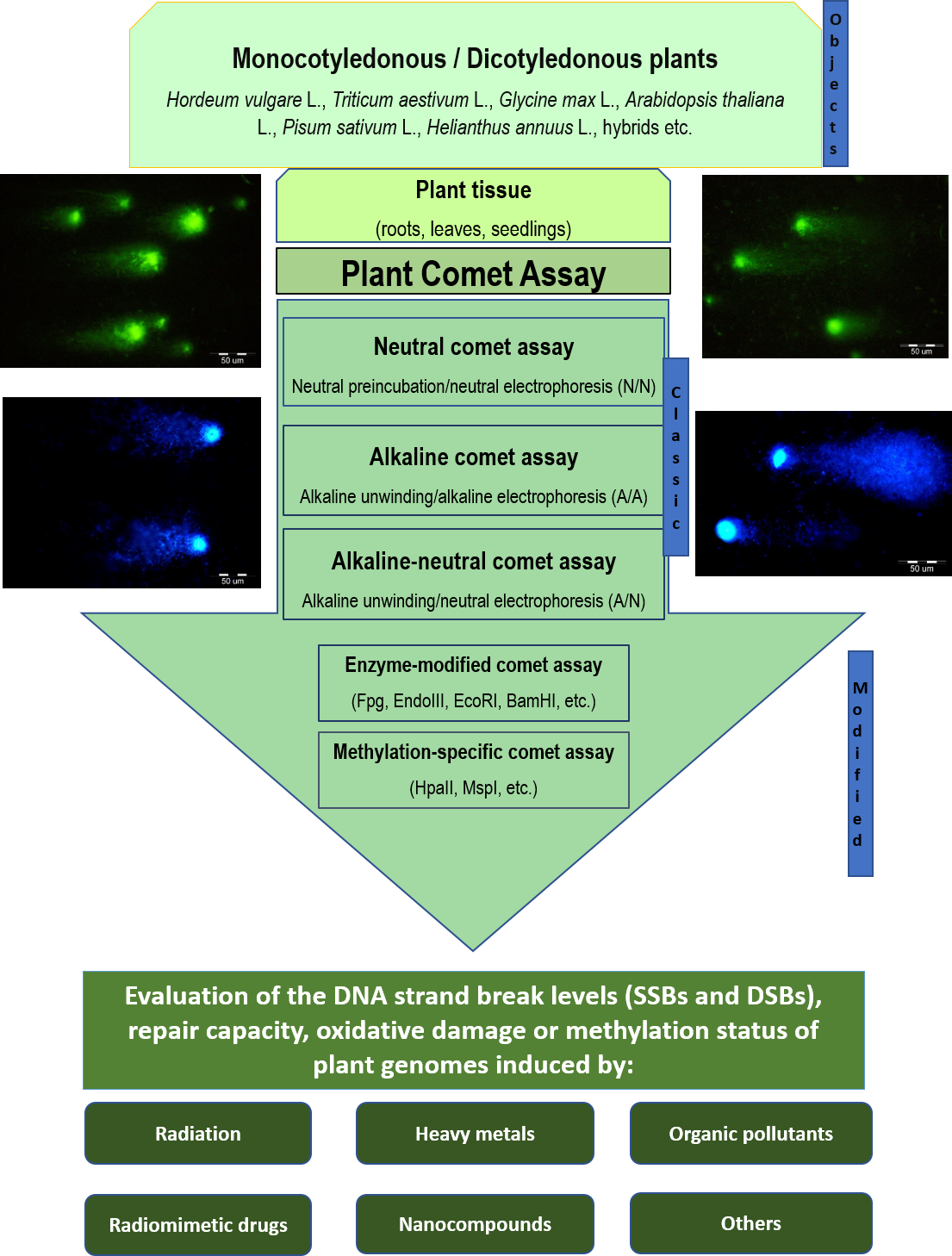
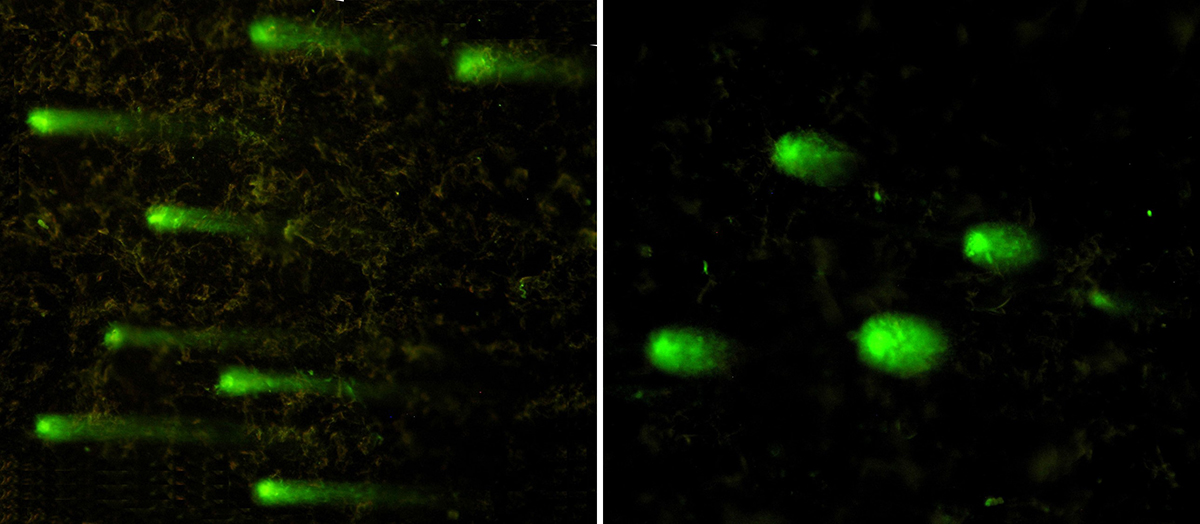
Неутрален кометен анализ върху изолирани ядра от грах, облъчени с UV-C радиация.
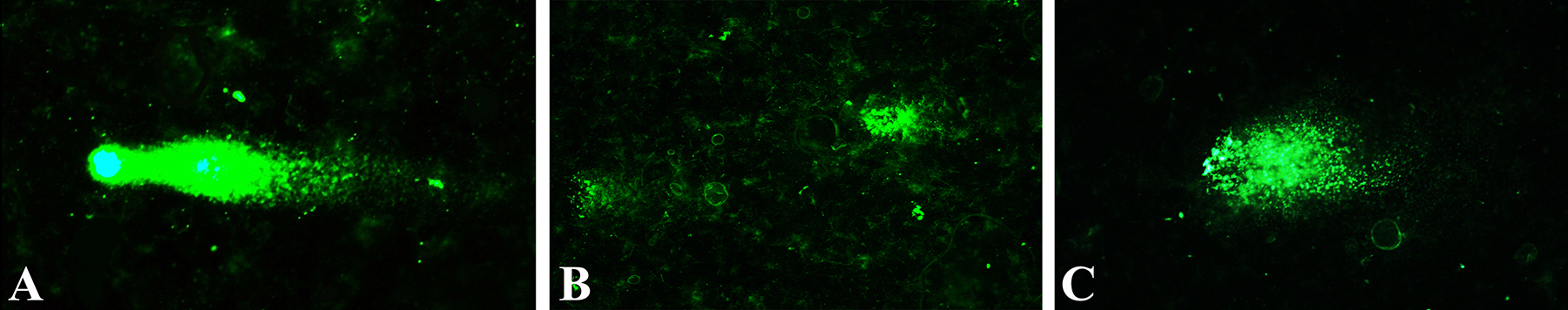
Индуцирани от радионуклиди ДНК повреди (едно- и двойно-верижни скъсвания) в изолирани ядра от соя, анализирани чрез алкален и алкално-неутрален кометен анализ.
Прочетете повече
- Georgieva M, Bonchev G, Zehirov G, Vasileva V, Vassileva V. 2021. Neonicotinoid insecticides exert diverse cytotoxic and genotoxic effects on cultivated sunflower. Environmental Science and Pollution Research 28, 53193-5320
- Georgieva M, Rashydov NM, Hajduch M. 2017. DNA damage, repair monitoring and epigenetic DNA methylation changes in seedlings of Chernobyl soybeans. DNA repair 50, 14-21.
- Georgieva M, Nikolova I, Bonchev G, Katerova Z, Todorova D. 2015. A comparative analysis of membrane intactness and genome integrity in pea, barley and wheat in response to UVC-irradiation. Turkish Journal of Botany 39, 6, 1008-1013.
- Stoilov L, Georgieva M, Manova V, Liu L, Gecheff K. 2013. Karyotype reconstruction modulates the sensitivity of barley genome to radiation-induced DNA and chromosomal damage. Mutagenesis 28, 2, 153-160.
- Georgieva M, Stoilov L, Rancheva E, Todorovska E, Vassilev D. 2010. Comparative аnalysis of data distribution patterns in plant comet assay. Biotechnology & Biotechnological Equipment 24, 4, 2142-2148.
- Georgieva M, Stoilov 2008. Assessment of DNA strand breaks induced by bleomycin in barley by the comet assay. Environmental and Molecular Mutagenesis 49, 5, 381-387.
[ Top ]
Молекулна и фенотипна характеристика на растенията в условия на абиотичен стрес
Молекулни и фенотипни маркери за изследване на генетичните основи на толерантността на растенията към абиотичен стрес
Изследва се ефектът на различни абиотични стресови фактори върху преживяването и продуктивността на растенията, както и защитните механизми, с които растенията противодействат на приложения стрес. Целта е да се разбере как някои генотипове се адаптират към променените условия на средата и защо един генотип е толерантен, а друг – чувствителен към стрес.
Генотип-зависими физиологични, биохимични, молекулярни, генетични и епигенетични промени в пшенични растения при засушаване (Agriculture, 2023, 13, 1823)
За анализите се използват физиолого-биохимични, молекулярно-генетични и морфологични маркери:
- Белтъчни маркери: профили на изоензими и резервни белтъци; променено ниво на Рубиско (рибулозо-1,5-бисфосфаткарбоксилаза/оксигеназа), Рубиско-свързващ белтък, Рубиско активаза, протеини на топлинния стрес, дехидрини, протеази и ензими, включени в защитата на растителните клетки от окислителен стрес.
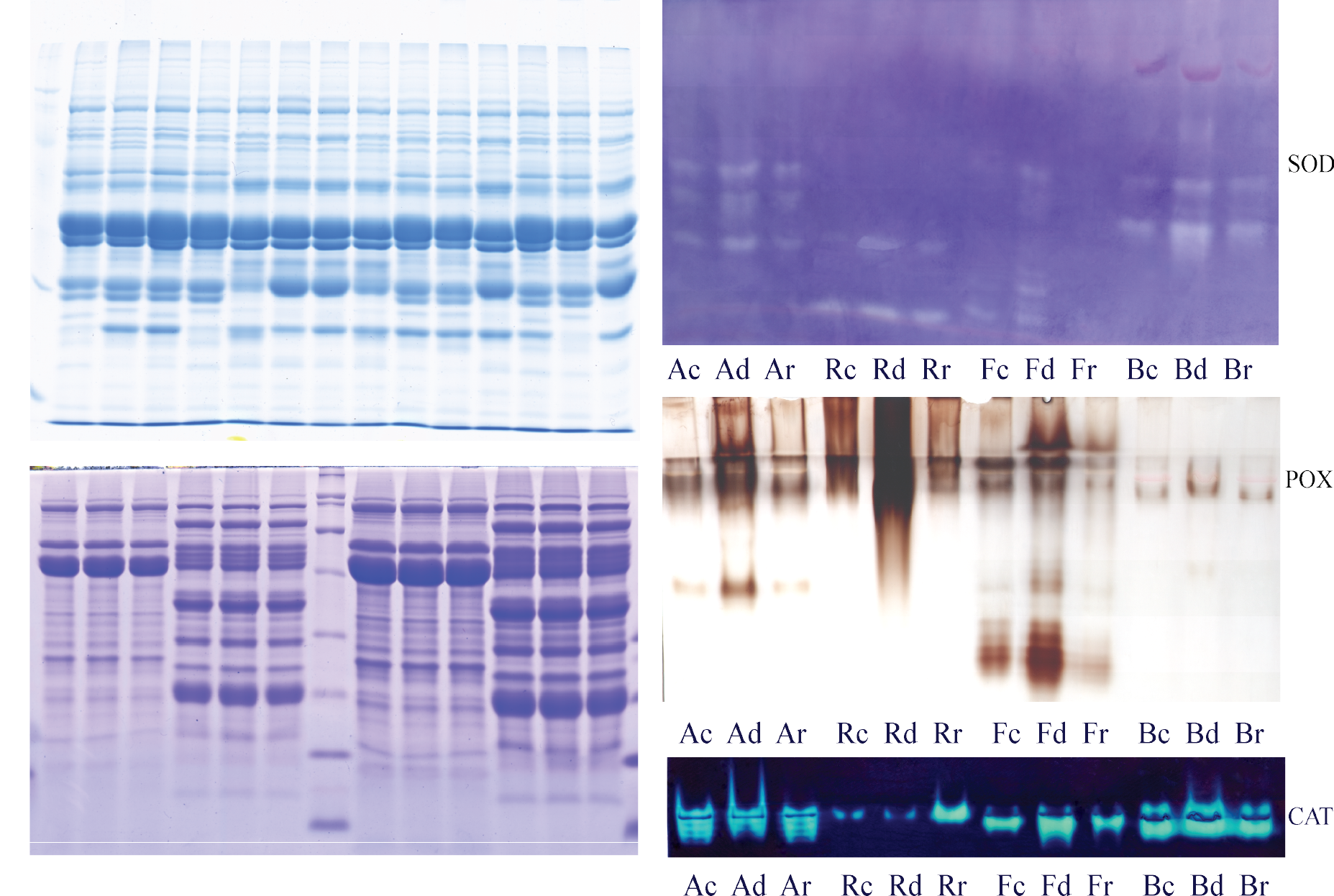
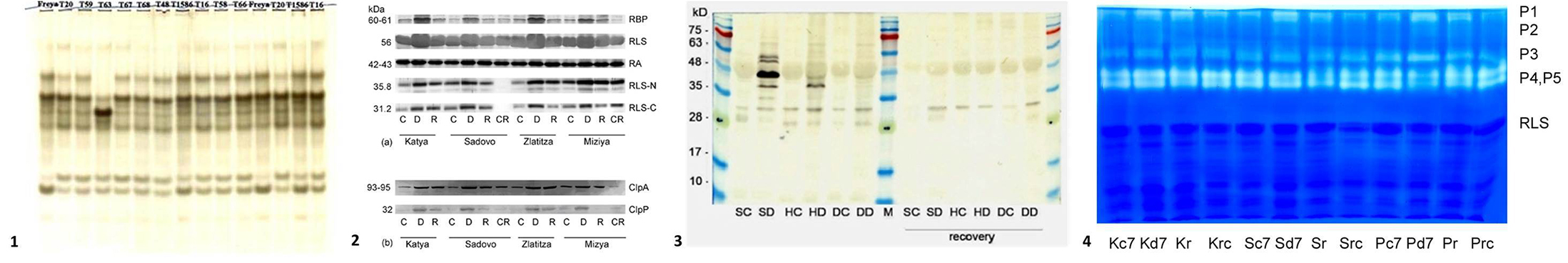
1 – Изоензимен профил на естерази от мутантни линии ечемик; 2 – Имуноблот анализ на екстракти от сортове пшеница с различна устойчивост към засушаване; 3 – Имуноблот анализ на дехидрини в Trifolium; 4 – Протеазна активност в гел на сортове пшеница с различна устойчивост към засушаване.
- Генни маркери: анализ на нивото на експресия на стрес-индуцируеми гени при различни типове абиотичен стрес.
- Фенотипни маркери: листно и кореново фенотипиране, микроморфология на растителни органи, подложени на абиотичен стрес.

Прочетете повече
- Georgieva M, Vassileva V. Stress management in plants: examining provisional and unique dose-dependent responses. International Journal of Molecular Sciences, 24, 6, 5105.
- Vassileva V, Georgieva M, Zehirov G, Dimitrova A. 2023. Exploring the genotype-dependent toolbox of wheat under drought stress. Agriculture, 13, 1823.
- Kirova E, Pecheva D, Simova-Stoilova L, 2021. Drought response in winter wheat – protection from oxidative stress and mutagenesis effect. Acta Physiologiae Plantarum 43, 8.
- Simova-Stoilova L, Pecheva D, Kirova E, 2020. Drought stress response in winter wheat varieties – changes in leaf proteins and proteolytic activities. Acta Botanica Croatica 79, 2, 129-138.
- Simova-Stoilova L, Vassileva V, Feller U, 2016. Selection and breeding of suitable crop genotypes for drought and heat periods in a changing climate: which morphological and physiological properties should be considered? Agriculture 6, 26, doi:10.3390/agriculture6020026.
- Vaseva I, Zehirov G, Kirova E, Simova-Stoilova L. 2016. Transcript profiling of serine- and cysteine protease inhibitors in Triticum aestivum varieties with different drought tolerance. Cereal Research Communications 44, 1, 79–88.
- Vaseva I, Anders I, Yuperlieva-Mateeva B, Nenkova R, Kostadinova A, Feller U. 2014. Dehydrin expression as a potential diagnostic tool for cold stress in white clover. Plant Physiology and Biochemistry, 78, 43-48.
- Vaseva I, Anders I, Feller U. 2014. Identification and expression of different dehydrin subclasses involved in the drought response of Trifolium repens. Journal of Plant Physiology, 171, 3-4, 213-224.
- Todorovska E, Dimitrova A, Stoilov L, Christov N, Vassilev D, Gecheff K. 2013. Molecular variability in barley structural mutants produced by gamma-irradiation. Plant Mutation Rep. 3, 1, 4-8.
- Georgieva M, Gecheff K. 2013. Molecular cytogenetic characterization of a new reconstructed barley karyotype. Biotechnology & Biotechnological Equipment 27, 1, 3577-3582.
- Vassileva V, Demirevska K, Simova‐Stoilova L, Petrova T, Tsenov N, Feller U. 2012. Long-term field drought affects leaf protein pattern and chloroplast ultrastructure of winter wheat in a cultivar specific manner. Journal of Agronomy and Crop Science 198, 2, 104–117.
- Grigorova B, Vassileva V, Klimchuk D, Vaseva I, Demirevska K, Feller U. 2012. Drought, high temperature, and their combination affect ultrastructure of chloroplasts and mitochondria in wheat (Triticum aestivum) leaves. Journal of Plant Interactions 7, 3, 204-213.
- Grigorova B, Vaseva I, Demirevska K, Feller U. 2011. Combined drought and heat stress in wheat: changes in some heat shock proteins. Biologia Plantarum 55, 1, 105-111.
- Grigorova B, Vaseva I, Demirevska K, Feller U. 2011. Expression of selected heat shock proteins after individually applied and combined drought and heat stress. Acta Physiologiae Plantarum 33, 5, 2041-2049.
- Vassileva V, Signarbieux C, Anders I, Feller U. 2011. Genotypic variation in drought stress response and subsequent recovery of wheat (Triticum aestivum ). Journal of Plant Research 124, 1, 147-154.
- Vaseva I, Akiscan Y, Demirevska K, Anders I, Feller U. 2011. Drought stress tolerance of red and white clover–comparative analysis of some chaperonins and dehydrins. Scientia Horticulturae, 130, 3, 653-659.
- Vaseva I, Sabotič J, Šuštar-Vozlič J, Meglič V, Kidrič M, Demirevska K, Simova-Stoilova L. 2011. The response of plants to drought stress: the role of dehydrins, chaperones, proteases and protease inhibitors in maintaining cellular protein function. Droughts: New Research, Nova Science Publishers, 1-45
- Simova-Stoilova L, Vaseva I, Grigorova B, Demirevska K, Feller U. Proteolytic activity and cysteine protease expression in wheat leaves under severe soil drought and recovery. Plant Physiology and Biochemistry 48, 2-3, 200-206.
- Vaseva I, Grigorova B, Simova-Stoilova L, Demirevska K, Feller U. 2010. Abscisic acid and late embryogenesis abundant protein profile changes in winter wheat under progressive drought stress. Plant Biology, 12, 5, 698-707.
- Vassileva V, Simova-Stoilova L, Demirevska K, Feller U. 2009. Variety-specific response of wheat (Triticum aestivum) leaf mitochondria to drought stress. Journal of Plant Research 122, 4, 445-454.
- Demirevska K, Zasheva D, Dimitrov R, Simova-Stoilova L, Stamenova M, Feller U. 2009. Drought stress effects on Rubisco in wheat: changes in the Rubisco larges ubunit. Acta Physiol. Plantarum 31, 1129-1138.
- Dimitrova А, Todorovska E, Christov NK, Stoilov L, Atanassov A, Gecheff K. 2008. Molecular characterization of structural barley mutants produced by gamma-irradiation. Genetics and Breeding, 37, 3-4, 15-26.
- Demirevska K, Simova-Stoilova L, Vassileva V, Vaseva I, Grigorova B, Feller U. 2008. Drought induced leaf protein alterations in sensitive and tolerant wheat varieties. General and Applied Plant Physiology, Special Issue 34, 1-2, 79-102.
- Demirevska K, Simova-Stoilova L, Vassileva V, Feller U. 2008. Drought response of Rubisco and some ATP-dependent chaperone proteins in wheat plants. Plant Growth Regulation 56, 97–106.
- Kirova E, Tzvetkova N, Vaseva I, Ignatov G. 2008. Photosynthetic responses of nitrate-fed and nitrogen-fixing soybeans to progressive water stress. Journal of Plant Nutrition 31, 445–458.
- Stoilova T, Dimitrova A, Angelova T, Gecheff K. 2006. Assessment of the genetic diversity in barley mutant lines using biochemical markers. Genetics and Breeding 35, 3-4, 3-10.
[ Top ]
Изменения в количеството и активността на ключови белтъци при стресови въздействия. Протеомен анализ.
Белтъците участват пряко във всички процеси, засягащи клетъчната структура и функция, и в приспособяването към измененията в околната среда, което е в основата на фенотипната пластичност. Белтъчният състав на клетката е променлив и невинаги съответства на състава на транскриптите, поради сложната регулация на генната експресия. Създаването на бази данни с частично/напълно секвенирани растителни геноми и експресиращи се последователности, както и на референтни протеомни карти, съществено улеснява използването на протеомни изследвания в търсене на подходящи белтъчни маркери за асистирана селекция. Двумерната електрофореза в комбинация с мас-спектрометрия улавя предимно белтъци, които количествено са по-добре застъпени, каквито са много от ключовите метаболитни ензими. По този начин се получава информация за основни биологични процеси, засегнати от стреса, както и за изоформи и пост-транслационни модификации. По-добро покритие на протеома, особено за по-слабо представените като количество белтъци (напр. със сигнална, транспортна функция), се постига с второ поколение протеомика (shotgun), като двата подхода са взаимно допълващи се.

Представителен двумерен гел с белтъчен профил на листен екстракт от детелина. Петната, най-засегнати от приложения стрес (заблатяване), се обозначени с номера и са идентифицирани с мас-спектрометрия (Stoychev et al Advances in Environmental Research. Vol. 39, 2015, 131-162).
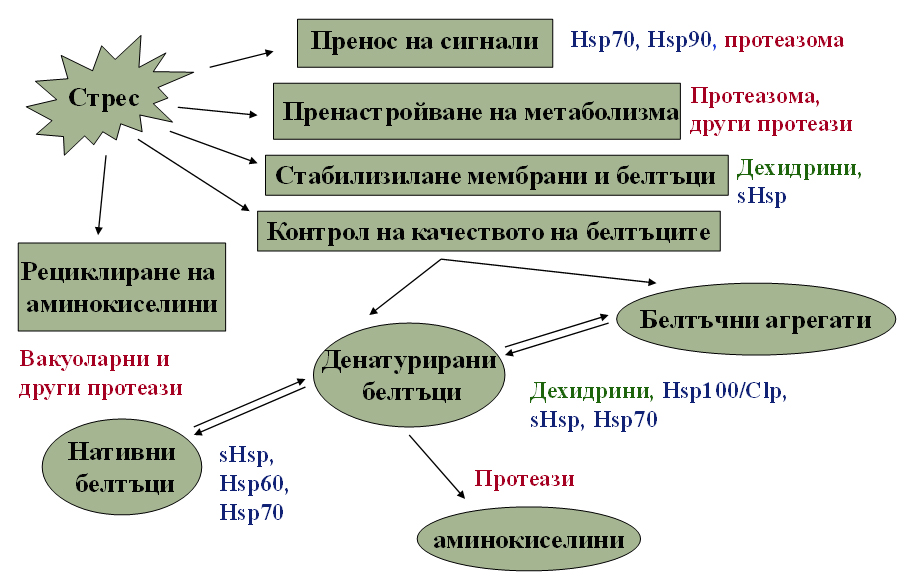
Абиотичните стресове с дехидратационен компонент (засушаване, засоляване, измръзване) имат негативно въздействие върху белтъчния състав на клетката. Наблюдава се увеличено количество на денатурирани, агрегирани и окислително увредени белтъци. Съществува система за контрол на качеството на белтъците, която се мобилизира при стрес и е жизнено важна за оцеляването в стресови условия. Тя отговаря за поддържането на белтъците във функционално активна конформация, предотвратява агрегирането на ненативни белтъци, възстановява нативната конформация или отстранява нефункциониращи и потенциално вредни за клетката белтъци. При стрес се синтезират защитни белтъци като дехидрини и различни видове шаперони, а необратимо увредените белтъци се разграждат от цял набор протеази. Активността на протеазите се контролира в известна степен от вътреклетъчни протеазни инхибитори. В условия на подтисната фотосинтеза разграждането на ненужни и запасни белтъци допълнително захранва метаболизма с градивни блокчета и източници за АТФ. Някои протеини от системата за контрол на качеството на белтъците са потенциални биохимични маркери за устойчивост към стрес.
Прочетете повече
- Simova-Stoilova LP, López-Hidalgo C, Sanchez-Lucas R, Valero-Galvan J, Romero-Rodríguez C, Jorrin-Novo JV. 2018. Holm oak proteomic response to water limitation at seedling establishment stage reveals specific changes in different plant parts as well as interaction between roots and cotyledons. Plant Science, 276: 1-13.
- Simova-Stoilova L, Vassileva V, Feller U. 2016. Selection and breeding of suitable crop genotypes for drought and heat periods in a changing climate: which morphological and physiological properties should be considered? Agriculture 6, 26, doi:10.3390/agriculture6020026
- Simova-Stoilova LP, Romero-Rodriguez MC, Sánchez-Lucas R, Navarro-Cerrillo RM, Medina- Auñón A, Jorrin-Novo JV. 2015. 2-DE proteomics analysis of drought treated seedlings of Quercus ilex supports a root active strategy for metabolic adaptation in response to water shortage. Frontiers in Plant Science 6, 627.
- Stoychev V, Simova-Stoilova L, Vassileva V, Jorrín Novo JV, Vaseva I, Velikova V, Tsonev T, Demirevska K. 2015. Changes in 2-DE Protein Profile of White and Red Clover Leaves in Response to Waterlogging Stress and Recovery. Advances in Environmental Research 39, 131-162. Ed. Justin A. Daniels, Nova Sci Publ. New York.
- Vaseva II, Anders I, Feller U. 2014. Identification and expression of different dehydrin subclasses involved in the drought response of Trifolium repens. Journal of Plant Physiology 171, 213–224.
- Vaseva II, Anders I, Yuperlieva-Mateeva B, Nenkova R, Kostadinova A, Feller U. 2014. Dehydrin expression as a potential diagnostic tool for cold stress in white clover. Plant Physiology and Biochemistry 78, 43-48.
- Stoychev V, Simova-Stoilova L, Vaseva I, Kostadinova A, Nenkova R, Feller U, Demirevska K. 2013. Protein changes and proteolytic degradation in red and white clover plants subjected to waterlogging. Acta Physiol. Plant. 35, 6, 1925-1932.
- Grigorova B, Vaseva I, Demirevska K, Feller U. 2011. Combied drought and heat stress in wheat: changes in some heat shock proteins. Plantarum 55, 1, 105-111.
- Grigorova B, Vaseva I, Demirevska K, Feller U. 2011. Comparative study of HSP expression after individualy applied and combined drought/heat stress in wheat plants. Acta Physiol. Plant. 33, 2041-2049.
- Vaseva I, Akiscan Y, Demirevska K, Anders I, Feller U. 2011. Drought stress tolerance of red and white clover – comparative analysis of some chaperonins and dehydrins. Scientia Horticulturae 130, 653–659.
- Vaseva I, Sabotič J, Šuštar-Vozlič J, Meglič V, Kidrič M, Demirevska K, Simova-Stoilova L. 2011. Response of plants to drought stress – the role of dehydrins, chaperones, proteases and protease inhibitors in maintaining cellular protein functionIn: Neves DF& Sanz JD (Eds.) Droughts: New Research, Chapter 11, Nova Science Publishers, Inc.
- Simova-Stoilova L, Vaseva I, Grigorova B, Demirevska K, FellerU. 2010. Proteolytic activity and cysteine protease expression in wheat leaves under severe soil drought and recovery. Plant Phys. Biochem. 48, 2-3, 200-206.
- Vaseva I, Grigorova B, Simova-Stoilova L, Demirevska K, Feller U. 2010. Abscisic acid and late embryogenesis abundant protein profile changes in winter wheat under progressive drought stress. Plant Biology 12, 5, 698-707.
- Simova-Stoilova L, Demirevska K, Petrova T, Tsenov N, Feller U. 2009. Antioxidative protection and proteolytic activity in tolerant and sensitive wheat (Triticum aestivum) varieties subjected to long-term field drought. Plant Growth Regulation 58, 1, 107-117.